Y despejando la T: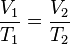
En la ley de Charles, las unidades de Tº son muy importantes, pues solo se puede medir en Kelvin (K).
Explicandolo según la teoria cineticomolecular: Si tenemos una cantidad de moleculas a una presión constante, y la temperatura aumenta 20ºC, estas empezarán a ir más rápido y presionando contra la pared del recipiente aumentando su volumen. Y si la Tº disminuye, las moleculas irán más despacio, ya no presionaran contra las paredes del recipiente, y provocarán la disminución de su volumen.


No hay comentarios:
Publicar un comentario